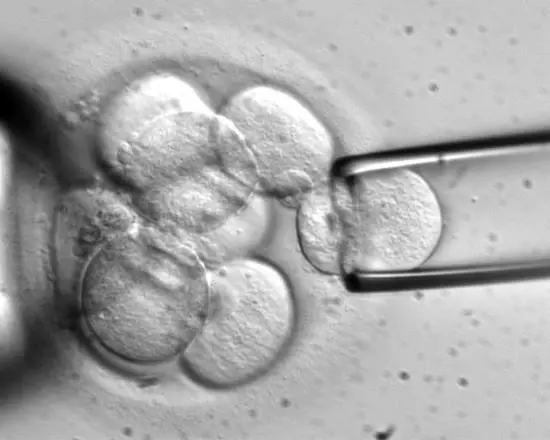
Significa poter cambiare le sorti di una vita, destinata a svilupparsi in un certo modo e invece riprogrammata perché alcuni aspetti genetici non vengano alla luce. Un traguardo importante che promette di curare le malattie geneticamente trasmissibili. Sono moltissime, almeno 10mila, e dipendono a volte da un solo gene che fa le bizze. Dunque, se noi fossimo in grado di zittirlo, il gioco sarebbe fatto. È questo il risultato di un team americano del Massachusetts Institute of Technology (Mit) di Boston. Gli embrioni sono stati trattati con una tecnica innovativa, la Crispr, da Clustered Regularly Interspaced Short Palidromic Repeats; che agisce sulla sequenza di basi azotate che uniscono i due filamenti del Dna. Adenina, guanina, citosina e timina, interagiscono fra loro attraverso particolari legami che possono essere rotti e ricostruiti imponendo una nuova sequenza nucleotidica. Alla base il tentativo di impedire l'azione di geni che a loro volta codificano proteine specifiche, molecole fondamentali per il buon funzionamento di un individuo.
Alcuni scienziati propongono la voce «editing del genoma»; e in effetti rende molto bene l'idea. È un po' come quello che accade in uno studio di registrazione quando si opera con software come Pro Tools o Cubase. Si tagliano e si inseriscono spezzoni musicali, ma in questo caso i soggetti non sono dei suoni, bensì dei geni. Crispr agisce in associazione a una proteina, la Cas9, in biologia importantissima per la risposta immunitaria batterica. Ma in laboratorio, grazie a una sequenza di Rna (l'altro acido nucleico che serve a produrre le proteine), possono agire in tandem, leggere il Dna di una specie e modificarlo. Spegnendo l'attività di una sequenza legata a una malattia genetica, o attivandone una nuova di zecca, concernente il potenziamento di un particolare meccanismo fisiologico.
È una tecnica che ricorda quella del Dna ricombinante, tarata per sostituire i geni malati; ma meno efficace di quest'ultima e meno precisa. Gli scienziati americani hanno svolto i loro test su embrioni di cinque giorni. È un momento delicato dello sviluppo, quello fra la morula e la blastocisti, due stadi che precedono la formazione dell'embrione vero e proprio, dal quale si origineranno tutti gli organi. In questo modo sono riusciti a indagare le caratteristiche genetiche dell'embrione in crescita e «spegnere» la sequenza che firma per la cardiomiopatia ipertrofica. È una patologia che determina un ispessimento delle pareti del cuore, provocata dal cattivo funzionamento delle proteine del sarcomero, necessarie all'autonomia delle fibre muscolari. Il fenomeno riguarda una persona su cento, e può causare improvvisi decessi per arresto cardiaco. È un male di grosso impatto perché chi ne soffre ha il 50% di chance di trasmettere il difetto genetico ai figli. Che da oggi, potenzialmente, possono essere trattati quando ancora non sono nati.
Tuttavia, come per il discorso della clonazione e dell'impiego di cellule staminali embrionali, anche in questo caso incombe il problema di natura etica. Di fatto con questa tecnica, e un budget nemmeno troppo consistente, è possibile creare individui con caratteristiche genetiche precise. E non vuol dire solo operare sull'uomo, ma anche su altre specie, che cambiando le loro caratteristiche, potrebbero impattare negativamente sul nostro divenire. Figuriamoci, un esempio banale, l'idea di zittire per sempre il ronzio delle zanzare, ritenute inutili scocciatrici.
Ma non è tutto così semplice, perché ogni specie ha un suo ruolo e un suo significato biologico; modificare anche solo un gene di un qualunque essere vivente, significa rompere questo idillio. E le conseguenze, al momento, non si possono nemmeno immaginare.
